
背景介绍
半月板损伤的再生修复目前依然充满挑战。近年来,随着再生医学和组织工程技术的发展,构建组织工程半月板支架实现半月板损伤的再生修复逐渐得到认可。理想的半月板组织工程支架应模拟天然半月板空间结构和微环境,有良好细胞相容性,有利于细胞生长和分化,促进损伤半月板的再生和修复。脱细胞基质由于具有仿生成分和天然微结构,在组织工程和再生医学中得到了广泛应用。其最大优点在于良好生物相容性,可很好地模拟细胞生长微环境,有效促进细胞生长和分化。本团队前期研究发现脱细胞半月板基质可有效促进细胞黏附、增殖和分化,进而促进损伤半月板再生修复,可以作为理想的生物材料。
3D打印技术可以实现高度个性化制造,准确制造出具备复杂结构的支架。然而,传统熔融沉积3D打印技术因打印过程中需要加热融化材料,故无法用于脱细胞半月板基质打印。 近年,低温沉积3D打印技术的出现为打印该材料提供了可能。该打印技术是在超低温(−30~ −20℃)平台上逐层搭建支架,经冷冻干燥和相分离技术实现支架高度连通的大孔-微孔结构。相对于传统熔融沉积3D打印技术,其具有以下优势:(1)超低温下完成打印,可以有效保护材料生物活性;(2)能构建具有高度连通的大孔-微孔结构,提高了支架孔隙率,这种分级多孔结构为细胞营养物质交换和扩散提供了通道。
本研究以脱细胞半月板基质为原料,通过低温沉积3D打印技术构建新型组织工程半月板支架,评价该支架理化特性和生物相容性,为其用于体内修复损伤半月板组织奠定基础。
方法
取新鲜猪膝关节半月板,采用改良物理化学联合方法脱细胞处理,获得脱细胞半月板基质匀浆;经大体观察、HE及DAPI染色观察脱细胞效果,甲苯胺蓝、番红O及天狼猩红染色评估黏多糖和胶原保留情况。然后制备脱细胞半月板基质生物墨水,通过低温沉积3D打印技术制备新型组织工程半月板支架。扫描电镜观察微观结构;与脂肪来源干细胞共培养后,采用细胞计数试剂盒8(cell counting kit 8,CCK-8)检测支架细胞相容性,死/活细胞染色和细胞骨架染色观察细胞活性和形态;植入大鼠皮下后组织学染色评估支架炎症细胞浸润与降解情况。
结果
大体观察半月板组织呈半月形或C形,脱细胞前呈乳白色纤维软骨样组织,质地柔软、有弹性;脱细胞半月板基质呈透明凝胶状。DAPI及HE染色示,脱细胞前半月板有大量细胞核结构,脱细胞处理后半月板基质未见细胞核结构,表明具有免疫原性的核酸组织彻底去除。番红O、甲苯胺蓝及天狼猩红染色示,脱细胞前后均呈阳性,提示脱细胞过程中黏多糖和胶原成分保留。
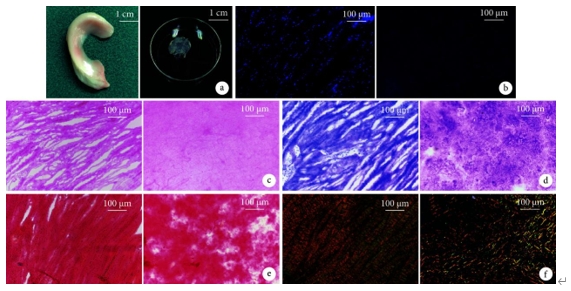
图1.半月板观察 左侧示脱细胞前,右侧示脱细胞后 a.大体观察;b. DAPI染色荧光显微镜观察;c. HE染色;d.番红O染色;e.甲苯胺蓝染色;f.天狼猩红染色
大体观察见新型组织工程半月板支架呈交叉网格状结构,纤维排列整齐。扫描电镜下可见支架具有明显纵横交错结构,大孔径(直径200~300 μm)分布较均匀,纤维径上微孔相互连接,微孔直径10~30 μm。(图2a,b)
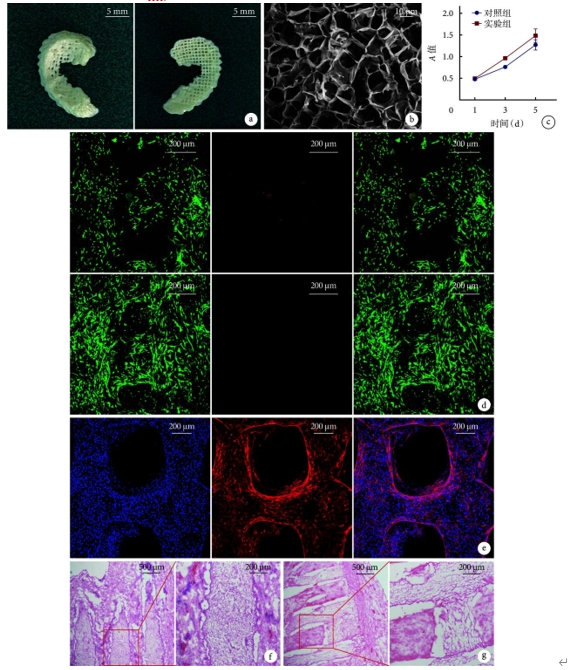
图2. 新型组织工程半月板支架观察 a.大体观察;b.扫描电镜观察;c. CCK-8检测细胞增殖;d.激光共聚焦显微镜下培养1天(上)及7天(下)死/活细胞染色观察 从左至右分别为活细胞染色、死细胞染色及两者重叠;e.激光共聚焦显微镜观察培养 7天鬼笔环肽染色观察;f、g.大鼠皮下植入后1、3周HE染色观察。
CCK-8检测示两组A值均随时间延长而增加,其中培养3、5天时实验组A值大于对照组,差异有统计学意义(P<0.05)(图2c)。死/活细胞染色示,支架上细胞以活细胞为主,细胞活性达90 %以上(其中1天94 %、7天95 %)(图2d)。鬼笔环肽染色示培养7天后支架上细胞呈梭形、分布均匀(图2e)。支架埋植于大鼠背部皮下HE染色示,1周时支架内部和支架与组织交界处炎症细胞浸润,支架无明显降解;3周时未见明显炎症细胞浸润,支架有部分降解,支架体积和纤维直径较植入前减小。讨论
近年来,随着半月板组织工程技术的不断发展,体外、内半月板替代物研发取得了许多进展。然而,半月板复杂结构和功能以及有限血供使其再生修复依然充满挑战。半月板再生过程中,支架应具有合适理化特性的结构框架,以帮助宿主细胞黏附和迁移,同时良好的仿生结构可以提供一个良好再生微环境。3D打印技术为构建复杂结构和异质性半月板提供了技术支撑。本研究采用的低温沉积3D打印技术是近年发展起来的快速成型技术之一,它不仅基于快速沉积制造工艺,而且结合了相分离工艺。采用该技术构建的组织工程支架除了具有可控的大孔径外,在纤维径上还具有相互连接的微孔,这些微孔有利于细胞旁分泌,增强细胞生物学功能,在组织工程支架制备和复杂器官设计方面具有广阔应用前景。目前,应用于3D生物打印的生物墨水主要分为人工合成材料和天然生物材料。人工合成材料主要有聚羟基乙酸、聚羟基乙酸-聚乳酸复合物、聚乳酸等。它们虽然具有物理机械性能良好、可控性强、微结构可调节等优点,但亲水性差、对细胞吸附力弱以及生物相容性不理想。天然生物材料包括海藻酸钠、明胶、胶原蛋白、壳聚糖、纤维蛋白、透明质酸和脱细胞外基质。其中脱细胞外基质保留了大部分天然成分,无免疫原性,是促进细胞增殖和分化的理想生物材料。既往文献及本团队研究显示脱细胞半月板基质的多孔结构和各种功能分子能决定干细胞分化方向,可能进一步促进半月板再生。因此,本研究中我们选择开发具有可打印性和满足细胞相容性的脱细胞半月板基质生物墨水,并基于低温沉积3D打印技术构建结构和成分双仿生的新型组织工程半月板支架。
研究结果显示,脱细胞技术成功去除半月板组织中具有免疫原性的核酸组织,并很好地保留了基质生物活性成分,包括黏多糖和多种胶原蛋白;制备的脱细胞半月板基质具有可打印性,利用低温沉积3D打印技术成功构建新型组织工程半月板支架。扫描电镜观察示这种新型支架不仅具有纵横交错的纤维,类似天然半月板胶原排列,更重要的是纤维径上形成了直径10~30 μm的微孔,为细胞生长提供了黏附位点,也为细胞物质交换、废物排出提供了通道。既往研究也表明支架多孔结构有助于细胞增殖、分化。本研究CCK-8检测示随着时间推移,支架上细胞增殖明显更快、更多,死/活细胞染色示支架上细胞活性良好,只见少量死细胞,提示构建的支架具有良好细胞相容性。同时,细胞骨架染色示MSCs能很好地在支架上黏附和伸展,并保持干细胞形态。进一步将支架植入大鼠皮下观察,植入1周有轻度炎症反应,3周炎症反应逐渐减轻,并出现支架部分降解。这种早期炎症反应会募集巨噬细胞,通过调节巨噬细胞极化,促进组织再生修复。
结论
理想的半月板组织工程支架应模拟天然半月板空间结构和微环境,有良好细胞相容性,有利于细胞生长和分化,促进损伤半月板的再生和修复。因此,本研究成功制备脱细胞半月板基质生物墨水,并利用低温沉积3D打印技术构建一种具有大孔-微孔分级微观结构的新型组织工程半月板支架,其能为细胞生长、黏附和增殖提供良好微环境。未来需进一步探讨该支架在体外成软骨分化作用及体内修复损伤半月板组织的效果,为其用于半月板再生修复提供更多数据支持。参考文献
Chen Mingxue, Wu Jiang, Yin Han, Wei Xiang, Liu Shuyun, Guo Quanyi.Construction of a novel tissue engineered meniscus scaffold based on low temperature deposition three-dimenisonal printing technology.Chinese Journal of Reparative and Reconstructive Surgery, 2024, 38(6): 748-754.
doi: 10.7507/1002-1892.202402063
