大段骨缺损早期神经-血管网络难以重建是骨再生修复面临的几个关键挑战之一。近日,武汉理工大学的戴红莲教授通过3D打印双离子时序释放平台促进了骨缺损中神经-血管网络重建,该文章名为“3D-printed dual-ion chronological release functional platform reconstructs neuro-vascularization
network for critical-sized bone defect regeneration”,发表在Chemical Engineering Journal上。本研究设计了一种3D打印的含镁明胶微球和掺锌生物玻璃的α-磷酸三钙支架,用于重建大段骨缺损的神经-血管网络,用于适配神经和血管再生在骨缺损发生后立即开始,并在随后的成骨分化中起关键作用的生物学过程。结果表明,含镁明胶微球可以调节Mg²⁺的释放速率,实现Mg²⁺的早期完全释放,从而有效增强人脐静脉内皮细胞的血管生成能力和PC12细胞的神经再生能力,同时避免Mg²⁺高浓度对晚期成骨的潜在抑制。此外,掺锌生物玻璃确保了Zn²⁺的长期释放,从而促进了骨髓间充质干细胞的活性和成骨分化。在大鼠颅骨大段缺损模型中,3D打印的α-磷酸三钙支架显著增强了神经-血管网络密度,并在促进新骨形成方面表现出优异的性能。因此,该时序释放平台有望用于修复大段骨缺损,并为修复材料的设计提供指导。

背景介绍
大段骨缺损是骨科临床治疗中的难题。目前,常用的治疗方法包括自体移植、同种异体移植和人工骨移植等策略。自体移植策略被认为是“金标准”,其中一个重要原因是自体骨含有丰富的神经-血管网络。因此,人工骨移植不能实现理想的骨修复效果可能是因为忽视了神经-血管网络的快速早期重建。
血管化在大段骨缺损修复中起着重要作用,它在骨修复过程中提供营养和因子以避免骨组织坏死,并通过促进神经肽受体的早期表达加速骨缺损的修复。此外,血管化还为骨相关神经再生提供了理想的环境。同时,神经系统在骨组织工程中的有益作用也已得到了证实。骨缺损发生后,缺损部位的神经修复在24小时内达到高峰。神经纤维通过分泌神经肽如降钙素基因相关肽和Sema3A参与血管修复和成骨分化。
在本研究中,作者以3D打印的α-磷酸三钙(α-TCP)水泥支架作为基质材料,引入含镁的明胶微球(Mg-GMS)和掺锌的生物玻璃(Zn-BG),构建了具有双离子时序释放功能的3D打印α-TCP支架(TCP/Zn-BG/Mg-GMS)。Mg-GMS用于控制Mg2+的释放速度,以促进早期神经-血管化网络的重建。而Zn-BG则用于调节支架的初始pH值,并确保Zn2+的长期释放,以促进成骨作用。3D打印支架提供了机械支撑和互连孔结构。该研究证实了复合支架的血管化和神经化能力及其对成骨分化的影响。最后,在体内建立了8毫米的大鼠颅骨大段骨缺损模型并对支架功能进行验证(图1)。通过微计算机断层扫描(micro-CT)和组织切片染色,探讨了神经-血管化网络重建对成骨的影响。这一研究策略提供了一种具有双离子时时序释放功能的3D打印α-TCP支架,有望作为修复大段骨缺损的骨移植物,并揭示了神经-血管化网络重建在修复大段骨缺损中的作用。
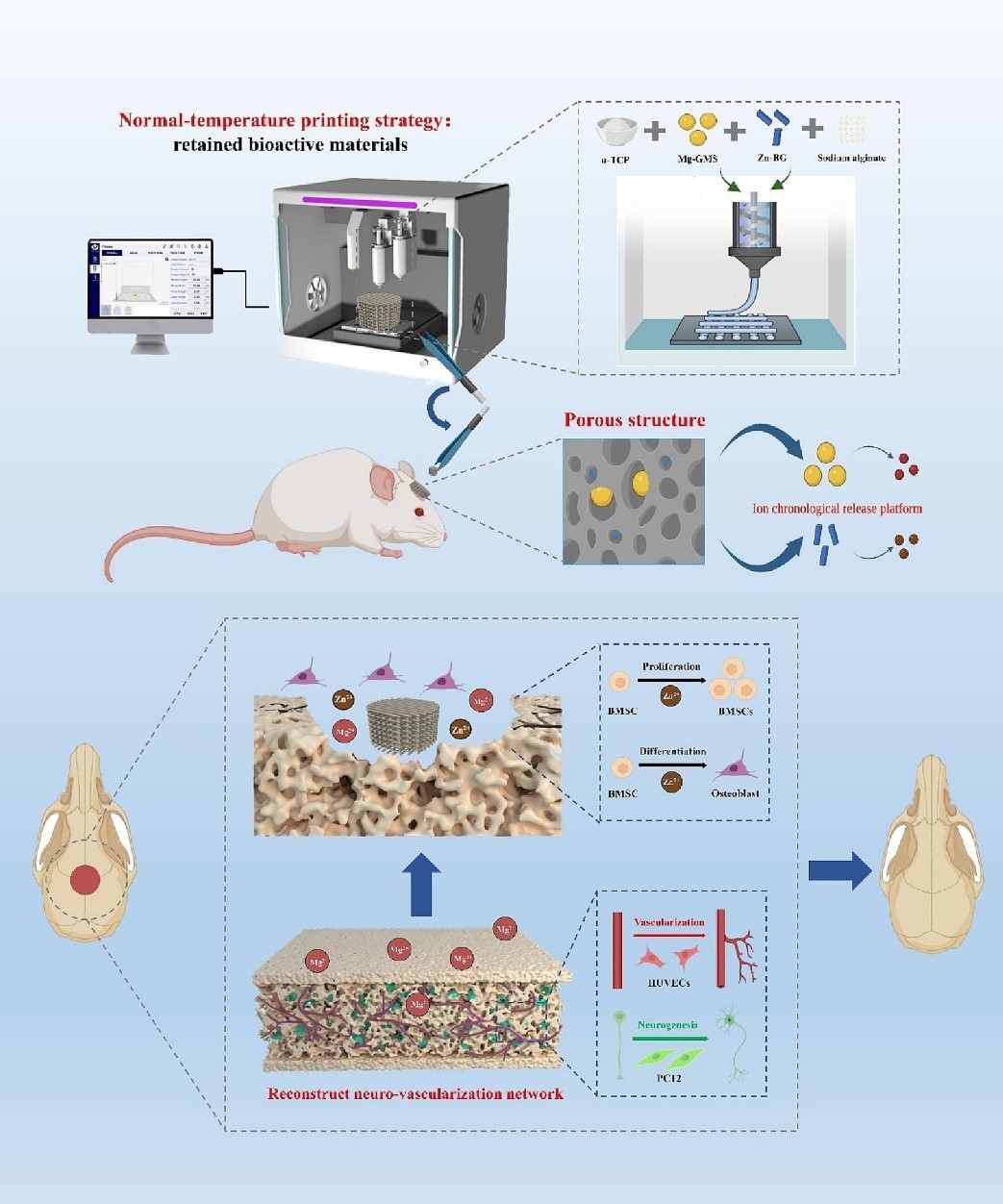
图1.3D打印的双离子释放支架,用于重建神经-血管化网络以促进骨再生
材料与方法
BG粉末通过溶胶-凝胶法制备。简而言之,将10.4 g TEOS、0.46 g TEP、1.52 g Ca(NO3)2·4H2O溶解在100 mL无水乙醇溶液中。然后在无水乙醇溶液中加入盐酸(0.5 mol/L)调节pH值,并使用Pluronic® F-127作为模板。混合溶液在40°C水浴中慢慢搅拌以蒸发溶剂。最后,将粉末在600°C下加热5小时得到BG。为了制备Zn-BG粉末,将10.4 g TEOS、0.46 g TEP、1.52 g Ca(NO3)2·4H2O、0.152 g Zn(NO3)2·6H2O溶解在100 mL无水乙醇溶液中,其余步骤相同。
Mg-GMS通过W/O乳化交联法制备。简而言之,在三颈烧瓶中加入30 mL液体石蜡和3 mL Span-80作为油相,并在50°C下以500 r/min搅拌混合。将葡萄糖酸镁和明胶按适当质量比(2:1和1:1)溶解在去离子水中,形成混合溶液作为水相。然后将5 mL混合溶液滴入油相中,保持连续搅拌。15分钟后,将反应转移到冰水浴(4℃)中,慢慢加入1 mL EDC溶液。反应1小时后停止,然后通过过滤分离所得的GMS,用异丙醇清洗,并在通风处干燥24小时。根据葡萄糖酸镁和明胶的比例,将样品分类为2:1 Mg-GMS组和1:1 Mg-GMS组。
将3 g α-TCP粉末和xBG(x= 0%、5%、10%、15%的质量比)粉末均匀混合。然后将海藻酸钠粉末加入去离子水中,制备10% w/v的海藻酸钠凝胶。将海藻酸钠凝胶加入到α-TCP和BG的粉末混合物中,通过机械搅拌直至形成糊状,得到打印墨水。通过3D打印机(SunP BioMaker 2)用混合浆料制作TCP/BG复合支架。3D打印喷嘴直径为500 μm,螺旋挤出速度为0.5–1 mm³/s,打印速度设定为5–15 mm/s,打印层厚度为500 μm。支架的主体打印完成后,将样品浸入10%磷酸溶液中进行5分钟的交联反应,然后用去离子水冲洗三次并在室温下干燥。
结果与讨论
明胶微球(GMS)因其良好的生物相容性和可控的降解性能,常被认为是理想的药物载体。Mg2+对神经-血管化网络的重建具有积极作用,但其治疗效果具有阶段依赖性。因此,有必要在早期释放Mg2+以促进神经-血管化网络的重建,而在后期不释放Mg2+以防止矿化。在本研究中,通过将镁和GMS按不同比例结合,调节Mg2+的释放浓度和时间。在第1天和第3天,2:1 Mg-GMS组的Mg2+释放浓度高于1:1 Mg-GMS组。而在第7天,两组均未释放Mg2+。结果证实,通过改变镁和GMS的复合比例,可以调节早期Mg2+的释放浓度,从而更有效地促进神经和血管的生长。另一方面,Mg2+的释放时间由GMS的降解时间决定,GMS的降解能力可以通过交联程度来调节。GMS的可控降解确保了Mg2+在一定时间内释放,而不会在后期阻碍矿化。根据先前的研究,两组Mg-GMS释放的Mg2+浓度均在安全范围内。因此,选择2:1 Mg-GMS组进行后续实验。
制备了不同粒径的Mg-GMS,以探索TCP/Mg-GMS打印墨水的打印能力。Mg-GMS的粒径可以通过改变搅拌速度来控制。当Mg-GMS的最大粒径大于500 μm时,打印过程中打印喷嘴会被Mg-GMS堵塞,导致打印过程中断。当Mg-GMS的最大直径小于300 μm时,打印支架的线条结构保持完整,且随着Mg-GMS的降解,表面出现了多级孔结构。因此,选择粒径小于300 μm的Mg-GMS进行后续实验。
先前的研究表明,Zn这一重要微量元素在骨重建中起着至关重要的作用。在成功制备TCP/BG复合支架的基础上,制备了TCP/Zn-BG复合支架。研究了Zn-BG在复合支架表面的分布情况。根据元素映射结果,发现Si、O和Zn均匀分布在复合支架的表面,表明Zn2+成功掺入BG中且Zn-BG分布均匀。基于上述实验,确定了BG的复合比例,并将Zn-BG制备为Zn2+释放平台。然后制备Mg-GMS,选择2:1 Mg-GMS组作为Mg2+释放平台。以3D打印磷酸钙水泥支架为基质材料,结合Zn-BG和Mg-GMS,形成3D打印双离子时间释放功能平台。与Mg-GMS在PBS中的直接释放相比,TCP/Zn-BG/Mg-GMS的Mg2+释放速率在前三天更加温和,释放时间也略有延长。但TCP/Zn-BG/Mg-GMS中的Mg2+仍可在早期完全释放。另一方面,Zn2+的释放时间可持续长达27天。
TCP/BG的抗压强度为15.44 ± 2.15 MPa,TCP/Zn-BG的抗压强度与之相比无显著变化。然而,TCP/Zn-BG/Mg-GMS的抗压强度下降至12.59 ± 1.38 MPa。TCP/Zn-BG/Mg-GMS机械性能下降的主要原因是添加Mg-GMS增加了支架的孔隙率。孔隙率的增加有助于提高骨整合,但往往以机械性能为代价。然而,TCP/Zn-BG/Mg-GMS的抗压强度仍满足松质骨的机械要求(4–12 MPa)。此外,通过调整GMS的含量,可以在很大范围内调节支架的表面孔结构。这使得支架可以根据不同骨缺损部位的特定结构和性能进行调整。在骨缺损修复和再生中,孔径大于50 μm有利于成骨质量提高,血管组织生长的最小孔径大于100 μm,微孔(孔径小于10 μm)有利于细胞粘附和蛋白质吸附。因此,在开发支架时,具有分级孔结构是一个重要考虑因素。在本研究中,通过BG和GMS的降解,在复合支架表面形成了微孔和大孔结构,并通过3D打印构建了互连孔结构。三组复合支架两个月内质量损失分别约为19 wt%、21 wt%和36 wt%。与TCP/BG和TCP/Zn-BG相比,TCP/Zn-BG/Mg-GMS具有更好的降解能力。材料的降解有助于新骨组织替代植入材料。
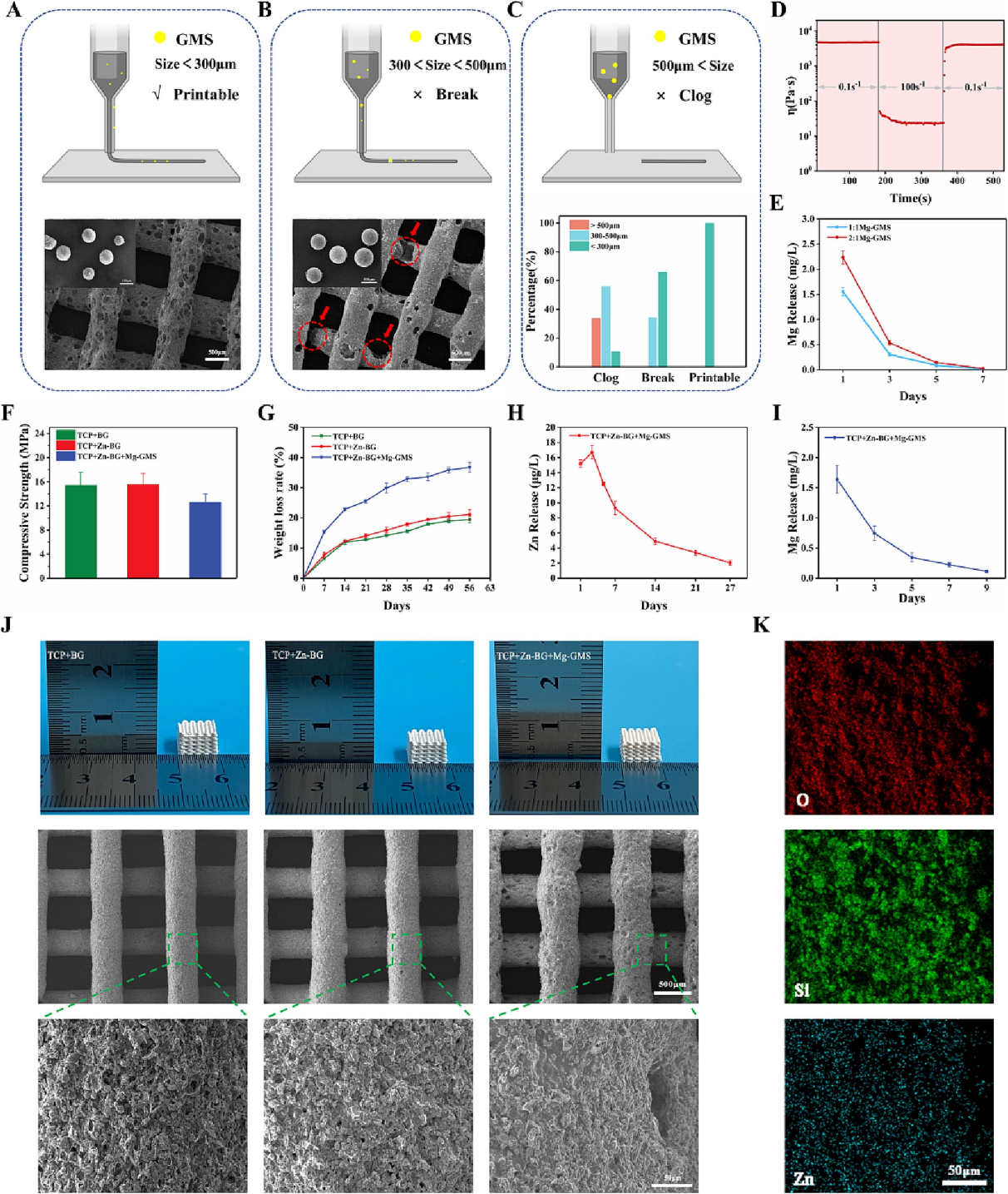
图2. 3D打印双离子时序释放支架的表征。(A - C)不同粒径Mg-GMS的TCP/Mg-GMS打印墨水的打印性测试。(D)TCP/Mg-GMS打印墨水的流变测试。(E)不同复合比例下的Mg2+释放动力学。(F)复合支架的抗压强度和(G)失重率。TCP/Zn-BG/Mg-GMS支架中Mg2+ (H) 和Zn2+ (I) 的释放动力学。(J)TCP/BG、TCP/Zn-BG和TCP/Zn-BG/Mg-GMS支架的SEM图像。(K)TCP/Zn-BG支架的EDS图谱。
骨组织中的血管网络为成骨提供了必需的营养、氧气和生长因子。因此,血管化对于支架的再生性能至关重要。接下来,研究检查了复合支架的血管生成能力。活/死细胞染色和CCK-8试验的结果显示,与其他两组相比,TCP/Zn-BG/Mg-GMS中的HUVECs细胞活力和增殖显著增加。Transwell试验用于测试HUVECs的迁移能力。TCP/Zn-BG/Mg-GMS中的迁移HUVECs数量显著高于其他两组。管状形成试验用于评估HUVECs的血管化过程。在TCP/Zn-BG/Mg-GMS中观察到较大的管状结构,与TCP/BG和TCP/Zn-BG形成鲜明对比,表明Mg2+从复合支架中释放后具有优异的血管生成活性。分支总长度的结果清楚地表明,TCP/Zn-BG/Mg-GMS中的计算参数远高于其他两组。这些结果进一步证实了TCP/Zn-BG/Mg-GMS对血管生长具有更好的诱导效果。总之,TCP/Zn-BG/Mg-GMS复合支架对血管网络的重建起到了积极作用。神经发生对于骨修复也至关重要。我们通过使用雪旺细胞(SCs)的活/死细胞染色和CCK-8试验,评估了三种复合支架的细胞相容性。结果显示,TCP/Zn-BG/Mg-GMS中的SCs数量显著高于其他两组。神经生长因子(NGF)和脑源性神经营养因子(BDNF)是调节神经生长的重要介质。RT-PCR分析用于评估这两种因子的表达。结果显示,与其他两组相比,TCP/Zn-BG/Mg-GMS表现出最高的基因表达。ELISA用于测定三组复合支架上种植的SCs的NGF分泌水平。结果显示,TCP/Zn-BG/Mg-GMS中的NGF分泌水平显著高于其他两组,表明Mg2+有利于神经修复。轴突萌发是外周神经再生的关键决定因素。因此,使用PC12细胞研究复合支架的轴突萌发能力,以评估神经再生能力。结果显示,TCP/BG和TCP/Zn-BG之间没有显著差异,而TCP/Zn-BG/Mg-GMS表现出最佳的神经突生长。上述结果表明,TCP/Zn-BG/Mg-GMS复合支架对血管和神经修复起到了积极作用。
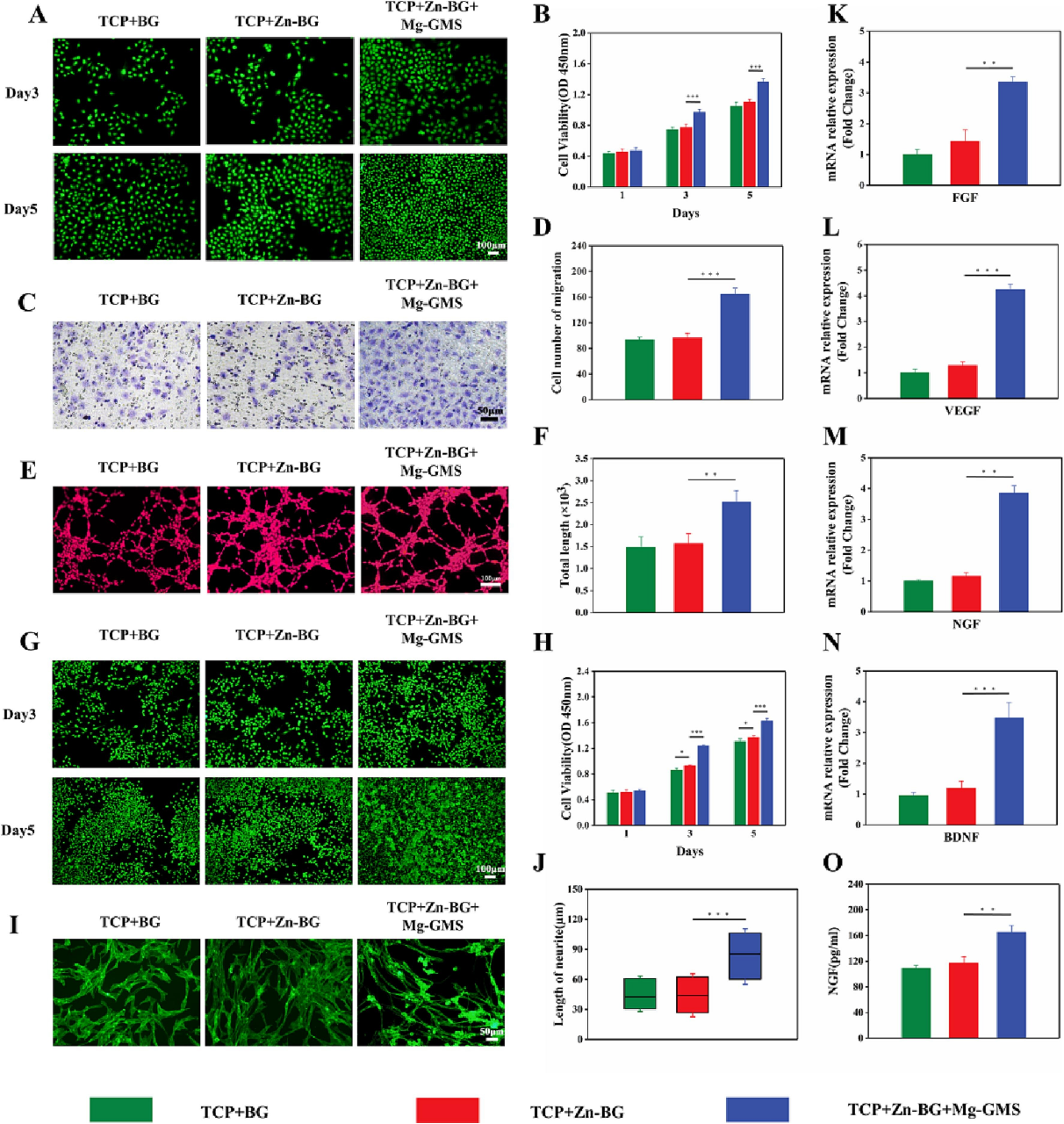
图3. 复合支架在体外促进血管化和神经再生的能力。体外通过活/死细胞染色(A)和CCK-8试验(B)评估HUVECs的活力和增殖。Transwell试验(C和D)测试HUVECs的迁移能力。管状形成试验(E)和分支总长度(F)评估HUVECs的血管化过程。体外通过活/死细胞染色(G)和CCK-8试验(H)评估SCs的活力和增殖。第5天PC12细胞的免疫染色图像(I)。神经突长度的定量分析(J)。(n = 15)。RT-PCR分析评估FGF(K)和VEGF(L)基因的表达。NGF(M)和BDNF(N)的RT-PCR分析。ELISA显示种植在复合支架上的SCs的NGF分泌(O)。*,P < 0.05;**,P < 0.01;***,P < 0.001。
研究通过使用8毫米的大鼠颅骨大段骨缺损模型,进一步研究了复合支架在体内的骨再生能力。使用micro-CT和组织学分析评估了第6周和第12周的骨恢复情况。与TCP/BG相比,TCP/Zn-BG有更多的新骨生长,表明Zn2+的长期释放有利于成骨,而TCP/Zn-BG/Mg-GMS在三组中对新骨生长的效果最好。新生骨组织的定量分析结果显示,TCP/Zn-BG/Mg-GMS的新生骨的骨体积分数(BV/TV)和骨密度(BMD)显著高于其他两组。通过组织学分析(H&E染色和MT染色),对新生骨组织进行了评估。所有组在植入后均未观察到明显的炎症反应或坏死。这些结果表明,TCP/Zn-BG/Mg-GMS中新骨组织的数量高于其他两组,表明TCP/Zn-BG/Mg-GMS具有更快和更好的骨再生能力。此外,从H&E和MT切片中发现,TCP/Zn-BG/Mg-GMS在支架内部有更多的骨组织生长。这表明通过Mg-GMS和BG的降解形成的多级孔结构有利于骨组织向支架内部生长,也表明这种多级孔结构有利于加速材料在体内的降解行为。这为新骨组织最终替代植入材料的可能性打开了大门。此外,从MT染色切片中发现,TCP/Zn-BG/Mg-GMS中的新生血管形成显著多于其他组,这与体外实验结果一致,表明TCP/Zn-BG/Mg-GMS能够促进血管化骨再生。
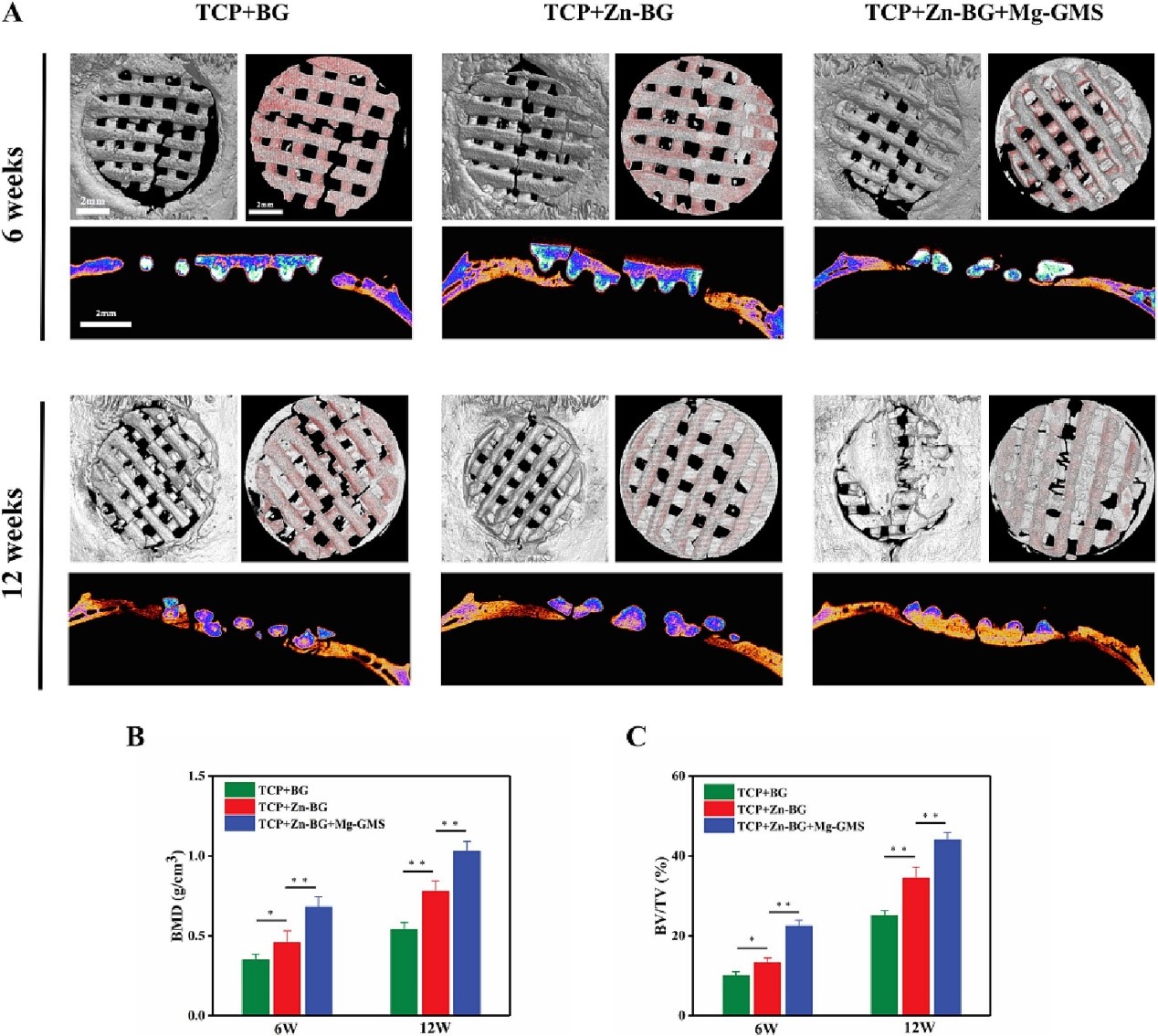
图4. 大鼠大段骨缺损的骨再生情况。术后第6周和第12周,(A)不同组在冠状面和矢状面上的典型CT重建图像。(B) 和 (C)颅骨大段骨缺损的微CT定量分析。*,P < 0.05;**,P < 0.01;***,P < 0.001。
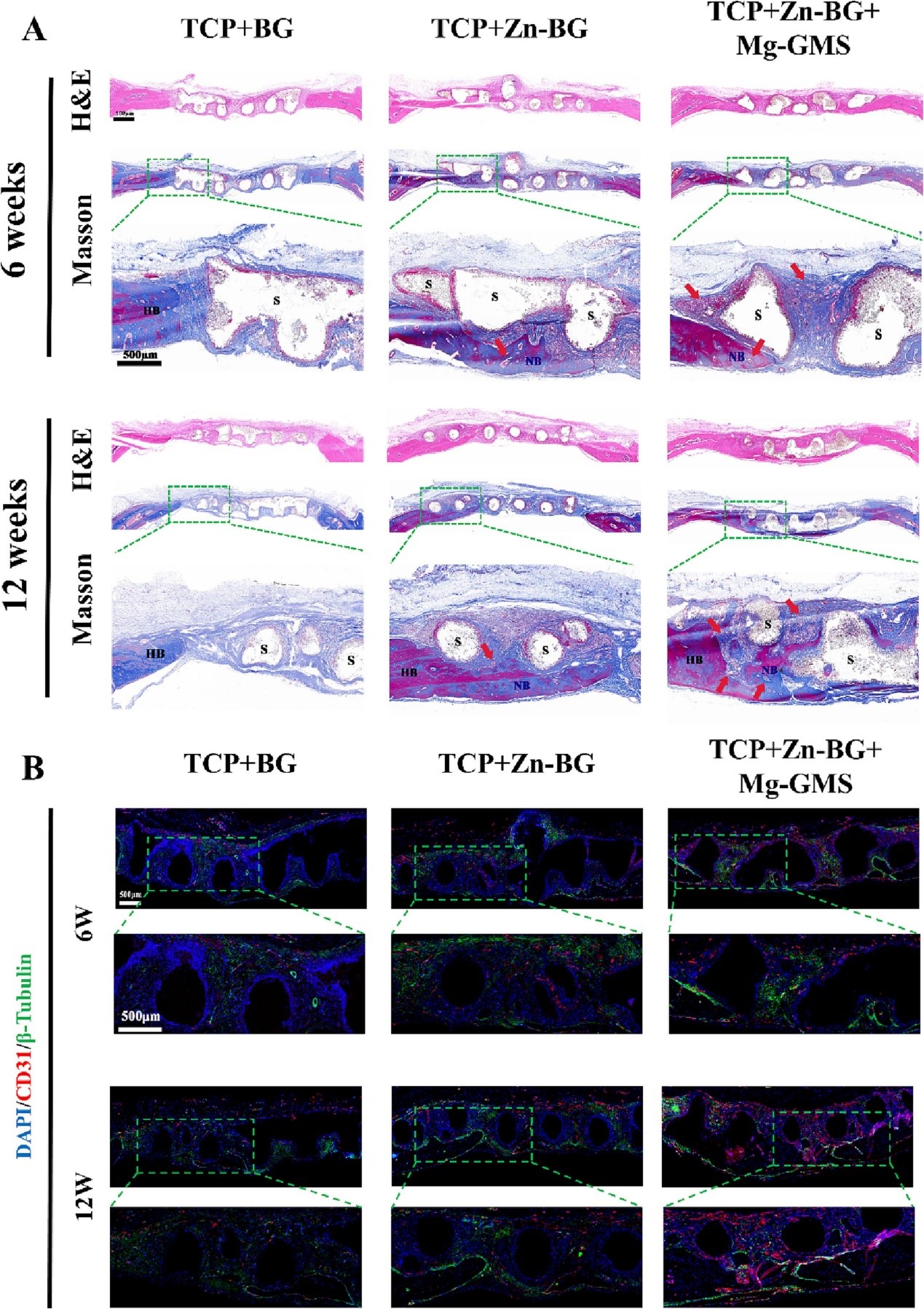
图7. 大鼠大段骨缺损的骨再生和神经-血管化。(A)H&E和MT染色。(B)从颅骨大段缺损样本中进行的CD31(血管,红色)和β3-微管蛋白(神经,绿色)共染色。
结论
在骨修复过程中,神经-血管化网络的重建在成骨过程中起着关键作用。因此,研究设计了一个3D打印的双离子时序释放功能平台,以重建神经-血管化网络,用于修复大段骨缺损。掺锌生物玻璃(Zn-BG)中Zn2+的长期释放能够有效上调Runx-2和OCN的表达,从而促进BMSCs的成骨分化。Mg-GMS可以调节Mg2+的释放时间和速度,有效激活VEGF和NGF的表达,以促进神经-血管化网络的重建。研究还使用该功能平台修复了大鼠的大段骨缺损。根据放射学和组织学检查,3D打印的双离子时序控释支架显著促进了早期血管化和神经发生,从而促进最终的骨再生和重塑。因此,上述支架有望用作修复大段骨缺损的骨移植物,并为修复材料的设计提供指导。
参考文献
Xia Y, Jing X, Wu X, et al. 3D-printed dual-ion chronological release functional platform reconstructs neuro-vascularization network for critical-sized bone defect regeneration[J]. Chemical Engineering Journal, 2023, 465: 143015.
https://doi.org/10.1016/j.cej.2023.143015
